FOXP3, T-Regulatorzellen und Autoimmunität – wie das Immunsystem seine „Bremse“ steuert
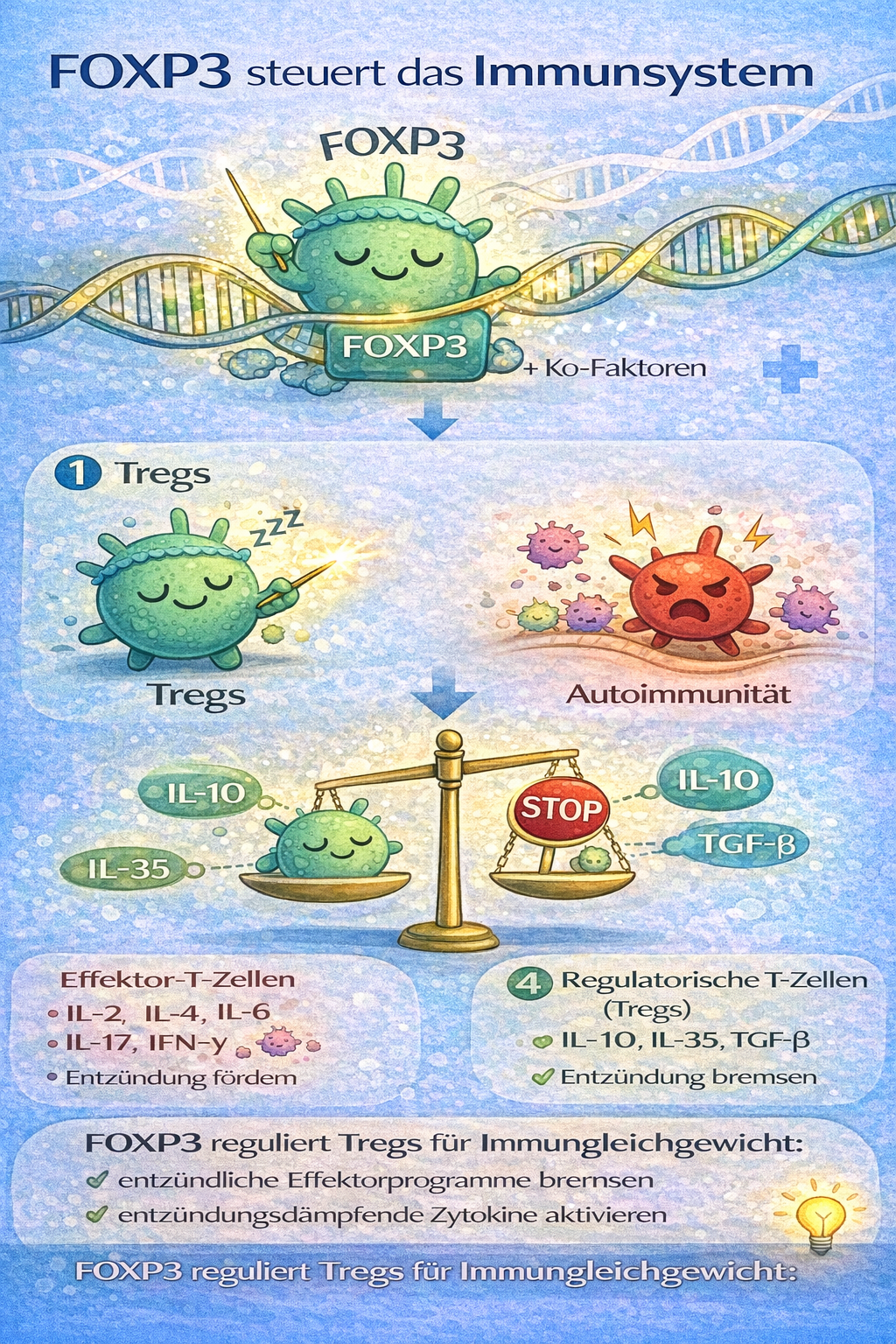
Unser Immunsystem ist ein Hochleistungssystem: Es erkennt Viren, Bakterien und Tumorzellen – und muss gleichzeitig lernen, körpereigene Strukturen in Ruhe zu lassen. Ein zentraler „Sicherheitsmechanismus“ dafür sind regulatorische T-Zellen (Tregs). Ihr wichtigster Taktgeber ist der Transkriptionsfaktor FOXP3. Wenn diese Achse gestört ist, steigt das Risiko für Autoimmunität – von schweren seltenen Syndromen bis zu häufigen Autoimmunerkrankungen.
FOXP3 – Dirigent der immunologischen Toleranz
FOXP3 ist der zentrale Transkriptionsfaktor regulatorischer T-Zellen (Tregs) und fungiert als molekularer „Dirigent“, der ein ganzes Orchester aus Genen koordiniert. Während Effektor-T-Zellen Immunreaktionen verstärken, sorgen FOXP3⁺ Tregs dafür, dass diese Reaktionen kontrolliert ablaufen und nicht gegen den eigenen Körper gerichtet sind. Wissenschaftlich betrachtet bindet FOXP3 an spezifische DNA-Sequenzen und steuert dort – gemeinsam mit Ko-Faktoren wie NFAT, RUNX1 oder STAT5 – die Aktivierung oder Repression zahlreicher Zielgene. Dadurch werden typische Suppressionsmechanismen ermöglicht, etwa die hohe Expression von CD25 (IL-2-Rezeptor-α), CTLA-4 oder immundämpfenden Zytokinen wie IL-10. Gleichzeitig unterdrückt FOXP3 Gene, die für starke entzündliche Effektorprogramme (z. B. Th1-, Th17- oder Th2-typische Zytokine) verantwortlich sind. So entsteht ein transkriptionelles Gegengewicht zur Entzündung.
FOXP3 schaltet somit bestimmte „Brems-Gene“ an und „Beschleunigungs-Gene“ aus.
Warum ist das wichtig?
Zu wenig Treg-Funktion (oder instabile Tregs) kann Autoimmunität und chronische Entzündung fördern. Zu viel „Bremse“ kann hingegen die Immunabwehr gegen Infektionen oder Tumoren schwächen.
Das Immunsystem braucht also Balance – nicht maximale Unterdrückung.
Woher kommen Tregs – und warum Stabilität (Epigenetik) so entscheidend ist Thymische vs. periphere Tregs
Ein großer Teil der Tregs entsteht im Thymus („natürliche“ Tregs). Weitere Tregs können sich in der Peripherie aus CD4⁺ T-Zellen entwickeln – besonders in tolerogenen Umgebungen wie dem Darm.
TSDR: Der „Stabilitäts-Schalter“ im FOXP3-Locus
Entscheidend ist nicht nur, dass das FOXP3-Gen vorhanden ist, sondern wie stabil es eingeschaltet bleibt.
In unseren Zellen gibt es chemische Markierungen an der DNA. Diese epigenetischen Markierungen wirken wie Schalter oder Sperren.
Beim FOXP3-Gen ist eine Region besonders wichtig: die Treg-specific demethylated region (TSDR).
- Demethylierte TSDR: FOXP3 bleibt dauerhaft aktiv. Die Zelle bleibt stabil regulatorisch – selbst unter entzündlichen Bedingungen.
- Unvollständige Prägung / (Re-)Methylierung: FOXP3 kann nur vorübergehend aktiv sein. Unter Entzündung kann die Zelle ihre regulatorische Funktion verlieren.
Das bedeutet:
FOXP3-Expression allein ist kein absoluter Garant für funktionelle Stabilität.
Man könnte sagen:
FOXP3 ist der Bauplan für die Immunbremse – die epigenetische Stabilität entscheidet, ob diese Bremse fest eingebaut oder nur locker angesetzt wurde.
Diese Stabilisierung beginnt bereits früh in der thymischen Treg-Entwicklung.
Wie Tregs unterdrücken: die wichtigsten Mechanismen
Tregs nutzen mehrere parallele Mechanismen:
- IL-2-Achse („Signal klauen“): Tregs exprimieren hoch CD25 (IL-2-Rezeptor-α). IL-2 ist essenziell für ihre Stabilität. Gestörtes IL-2-Signaling kann Treg-Dysfunktion und Autoimmunität fördern.
- Kontakt-abhängige Regulation (CTLA-4): CTLA-4 reduziert die Aktivierung antigenpräsentierender Zellen. Dadurch wird die nachgeschaltete Effektor-T-Zell-Aktivierung gedämpft.
- Antiinflammatorische Zytokine (IL-10 u. a.): Besonders in Schleimhäuten spielen IL-10 und andere immundämpfende Zytokine eine zentrale Rolle.
- Gewebe-Spezialisierung („effector Tregs“): Tregs passen sich organ-spezifischen Milieus an (Darm, Haut, Fettgewebe etc.). Diese Spezialisierung erhöht Schutz, kann unter Entzündung jedoch auch Plastizitätsprozesse begünstigen.
Wenn FOXP3/Tregs versagen
A) IPEX – das Lehrbuchbeispiel
FOXP3-Mutationen führen zu IPEX mit:
- früher schwerer Enteropathie
- Dermatitis
- Endokrinopathien (z. B. Typ-1-Diabetes)
IPEX zeigt kausal:
FOXP3-abhängige Treg-Funktion ist ein Grundpfeiler der Selbsttoleranz.
B) Häufigere Autoimmunerkrankungen
Hier liegt meist keine komplette FOXP3-Mutation vor, sondern eine Dysbalance:
- verminderte Treg-Zahl
- funktionelle Einschränkung
- ungünstiges Treg : Effektor-Verhältnis
- entzündliches Milieu mit verminderter Stabilität
Therapie-Ideen 2024–2026
- Low-dose IL-2: Selektive Expansion und Stabilisierung von Tregs.
- IL-2-Varianten (Muteins): Gezielte Modulation zugunsten von Tregs.
- Adoptive Treg-Zelltherapie: Ex-vivo expandierte oder antigenspezifische Tregs.
- IPEX: Hämatopoetische Stammzelltransplantation als kurativer Ansatz; neue gentherapeutische Strategien in Entwicklung.
Häufige Missverständnisse
- Sind Tregs immer gut?: Nein – zu viel Suppression kann Tumor- oder Infektabwehr schwächen.
- FOXP3 = Treg = immer stabil?: Nein – epigenetische Stabilität (TSDR) ist entscheidend.
- Autoimmunität = Treg-Mangel?: Meist eher funktionelle Dysbalance als absoluter Mangel.
Take-home-Message
- FOXP3⁺ Tregs sind das zentrale Bremssystem der Immunantwort.
- FOXP3 programmiert ein transkriptionelles Gegengewicht zur Entzündung.
- Epigenetische Stabilität (TSDR-Demethylierung) entscheidet über dauerhafte Funktion.
- IPEX beweist die essenzielle Rolle dieser Achse.
- Therapeutisch rückt die gezielte Stärkung von Tregs zunehmend in den Fokus.
___________________________________________________________________________________________________________________
Referenzen:
https://www.nature.com/articles/s41392-025-02326-4?utm_source=chatgpt.com
https://pubmed.ncbi.nlm.nih.gov/17917016/
https://onlinelibrary.wiley.com/doi/10.1111/imm.13178?utm_source=chatgpt.com
https://pubmed.ncbi.nlm.nih.gov/23420886/
https://academic.oup.com/jimmunol/article/193/6/2699/7960457?utm_source=chatgpt.com&login=false
https://www.mdpi.com/1422-0067/25/13/7171?utm_source=chatgpt.com
https://www.sciencedirect.com/science/article/pii/S2211124724012890?utm_source=chatgpt.com
https://pmc.ncbi.nlm.nih.gov/articles/PMC2248278/?utm_source=chatgpt.com
https://www.sciencedirect.com/science/article/pii/S2211124724012890?utm_source=chatgpt.com
https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2025.1511671/full?utm_source=chatgpt.com